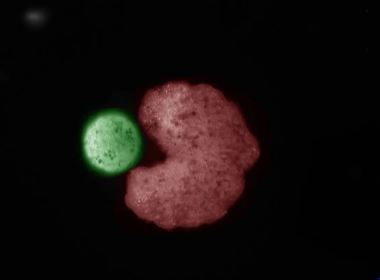
Estos xenobots pueden curarse y moverse por sí mismos y están desarrollados a partir de células de embrión de rana.
Basados en un algoritmo evolutivo, estos seres son mitad animal (rana), mitad robot y son los primeros robots vivos autorreplicantes de la historia.
Estos robots vivientes de tamaño milimétrico, llamadas Xenobots 3.0, no son robots tradicionales, sino organismos vivos programables. Hechos a partir de células vivas obtenidas de embriones de rana de uñas africanas (Xenopus laevis), los organismos diseñados por ordenador y creados por un equipo de cuatro científicos estadounidenses, reúnen células individuales dentro de una 'boca' que recuerda al videojuego Pac-Man y liberan 'bebés' que se ven y se mueven como sus progenitores.
Son formas de vida sintéticas que, a pesar de su genoma de rana, no son ranas. El modo de reproducirse es por replicación cinemática; algo que se ha visto a nivel molecular, pero nunca a esta escala. El diseño realizado en ordenador permitió una configuración vital para que estos robots vivos puedan realizar tareas como mover, empujar o transportar objetos. La IA realizó miles de millones de simulaciones para llegar a la configuración que finalmente funcionó.
Estos robots vivos autorreplicantes representan una investigación prometedora para los avances hacia la medicina regenerativa, según los científicos, ya que podrían permitir un tratamiento farmacológico más directo y personalizado para lesiones traumáticas, defectos de nacimiento, cáncer, envejecimiento y mucho más.
"Si supiéramos cómo decirle a las colecciones de células que hagan lo que queremos que hagan, en última instancia, esa es la medicina regenerativa, esa es la solución para las lesiones traumáticas, los defectos de nacimiento, el cáncer y el envejecimiento", comenta Michael Levin de la Universidad de Tufts y coautor del trabajo.
Sam Kriegman, Douglas Blackiston, Michael Levin, and Josh Bongard
PNAS December 7, 2021 118 (49) e2112672118; https://doi.org/10.1073/pnas.2112672118
Edited by Terrence J. Sejnowski, Salk Institute for Biological Studies, La Jolla, CA, and approved October 22, 2021 (received for review July 9, 2021)